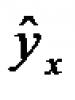Химия. Химия Количество энергетических уровней в атоме определяется
Рис. 7. Изображение форм и ориентаций
s -,p -,d -, орбиталей с помощью граничных поверхностей.
Квантовое число m l называют магнитным . Оно определяет пространственное расположение атомной орбитали и принимает целые значения от –l до +l через нуль, то есть 2l + 1 значений (табл. 27).
Орбитали одного подуровня (l = const) имеют одинаковую энергию. Такое состояние называют вырожденным по энергии . Так p -орбиталь – трехкратно, d – пятикратно, а f – семикратно вырождены. Граничные поверхности s -,p -,d -, орбиталей показаны на рис. 7.
s -орбитали сферически симметричны для любого n и отличаются друг от друга только размером сферы. Их максимально симметричная форма обусловлена тем, что при l = 0 и μ l = 0.
Таблица 27
Число орбиталей на энергетических подуровнях
|
Орбитальное квантовое число |
Магнитное квантовое число |
Число орбиталей с данным значением l |
|
m l | ||
|
–2, –1, 0, +1, +2 | ||
|
–3, –2, –1, 0, +1, +2, +3 |
p -орбитали существуют при n ≥ 2 и l = 1, поэтому возможны три варианта ориентации в пространстве: m l = –1, 0, +1. Все p-орбитали обладают узловой плоскостью, делящей орбиталь на две области, поэтому граничные поверхности имеют форму гантелей, ориентированных в пространстве под углом 90° друг относительно друга. Осями симметрии для них являются координатные оси, которые обозначаются p x , p y , p z .
d -орбитали определяются квантовым числом l = 2 (n ≥ 3), при котором m l = –2, –1, 0, +1, +2, то есть характеризуются пятью вариантами ориентации в пространстве. d -орбитали, ориентированные лопастями по осям координат, обозначаются d z ² и d x ²– y ² , а ориентированные лопастями по биссектрисам координатных углов – d xy , d yz , d xz .
Семь f -орбиталей , соответствующих l = 3 (n ≥ 4), изображаются в виде граничных поверхностей.
Квантовые числа n , l и m не полностью характеризуют состояние электрона в атоме. Экспериментально установлено, что электрон имеет еще одно свойство – спин. Упрощенно спин можно представить как вращение электрона вокруг собственной оси. Спиновое квантовое число m s имеет только два значения m s = ±1/2, представляющие собой две проекции углового момента электрона на выделенную ось. Электроны с разными m s обозначаются стрелками, направленными вверх и вниз.
Последовательность заполнение атомных орбиталей
Заселение электронами атомных орбиталей (АО) осуществляется согласно принципу наименьшей энергии, принципу Паулии правилу Гунда, а для многоэлектронных атомов – правилу Клечковского.
Принцип наименьшей энергии требует, чтобы электроны заселяли АО в порядке увеличения энергии электронов на этих орбиталях. Это отражает общее правило – максимуму устойчивости системы соответствует минимум ее энергии.
Принцип Паули (1925 г) запрещает в многоэлектронном атоме находиться электронам с одинаковым набором квантовых чисел. Это означает, что два любых электрона в атоме (или молекуле, или ионе) должны отличаться друг от друга значением хотя бы одного квантового числа, то есть на одной орбитали может быть не более двух электронов с различными спинами (спаренных электронов). Каждый подуровень содержит 2l + 1 орбитали, на которых размещаются не более 2(2l + 1) электронов. Отсюда следует, что емкость s -орбиталей – 2, p -орбиталей – 6, d -орбиталей – 10 и f -орбиталей – 14 электронов. Если число электронов при заданном l просуммировать от 0 до n – 1, то получим формулу Бора– Бьюри , определяющую общее число электронов на уровне с заданным n :
Эта формула не учитывает межэлектронное взаимодействие и перестает выполняться при n ≥ 3.
Орбитали с одинаковыми энергиями (вырожденные) заполняются в соответствии с правилом Гунда : наименьшей энергией обладает электронная конфигурация с максимальным спином. Это означает, что если на p-орбитали три электрона, то они располагаются так: , и суммарный спинS =3/2, а не так: ,S =1/2.
Правило Клечковского (принцип наименьшей энергии). В многоэлектронных атомах, как и в атоме водорода, состояние электрона определяется значениями тех же четырех квантовых чисел, однако в этом случае электрон находится не только в поле ядра, но и в поле других электронов. Поэтому энергия в многоэлектронных атомах определяется не только главным, но и орбитальным квантовым числом, а вернее их суммой: энергия атомных орбиталей возрастает по мере увеличения суммы n + l ; при одинаковой сумме сначала заполняется уровень с меньшим n и большим l . Энергия атомных орбиталей возрастает согласно ряду:
|
1s <2s <2p <3s <3p <4s ≈3d <4p <5s ≈4d <5p <6s ≈4f ≈5d <6p <7s ≈5f ≈6d <7p . |
Итак, четыре квантовых числа описывают состояние электрона в атоме и характеризуют энергию электрона, его спин, форму электронного облака и его ориентацию в пространстве. При переходе атома из одного состояния в другое происходит перестройка электронного облака, то есть изменяются значения квантовых чисел, что сопровождается поглощением или испусканием атомом квантов энергии.
Е.Н.ФРЕНКЕЛЬ
Самоучитель по химии
Пособие для тех, кто не знает, но хочет узнать и понять химию
Часть I. Элементы общей химии
(первый уровень сложности)
Продолжение. Начало см. в № 13, 18, 23/2007
Глава 3. Элементарные сведения о
строении атома.
Периодический закон Д.И.Менделеева
В с п о м н и т е, что такое атом, из чего состоит атом, изменяется ли атом в химических реакциях.
Атом – это электронейтральная частица, состоящая из положительно заряженного ядра и отрицательно заряженных электронов.
Число электронов в ходе химических процессов может изменяться, но заряд ядра всегда остается неизменным . Зная распределение электронов в атоме (строение атома), можно предсказать многие свойства данного атома, а также свойства простых и сложных веществ, в состав которых он входит.
Строение атома, т.е. состав ядра и распределение электронов вокруг ядра, несложно определить по положению элемента в периодической системе.
В периодической системе Д.И.Менделеева химические элементы располагаются в определенной последовательности. Эта последовательность тесно связана со строением атомов этих элементов. Каждому химическому элементу в системе присвоен порядковый номер , кроме того, для него можно указать номер периода, номер группы, вид подгруппы.
Спонсор публикации статьи интернет-магазин "Мегамех". В магазине Вы найдёте изделия из меха на любой вкус - куртки, жилетки и шубы из лисы , нутрии, кролика, норки, чернобурки, песца. Компания также предлагает Вам приобрести элитные меховые изделия и воспользоваться услугами индивидуального пошива. Меховые изделия оптом и в розницу - от бюджетной категории до класса люкс, скидки до 50%, гарантия 1 год, доставка по Украине, России, СНГ и странам Евросоюза, самовывоз из шоу-рума в г.Кривой Рог, товары от ведущих производителей Украины, России, Турции и Китая. Посмотреть каталог товаров, цены, контакты и получить консультацию Вы сможете на сайте, который располагается по адресу: "megameh.com".
Зная точный «адрес» химического элемента – группу, подгруппу и номер периода, можно однозначно определить строение его атома.
Период – это горизонтальный ряд химических элементов. В современной периодической системе семь периодов. Первые три периода – малые , т.к. они содержат 2 или 8 элементов:
1-й период – Н, Не – 2 элемента;
2-й период – Li … Nе – 8 элементов;
3-й период – Na ... Аr – 8 элементов.
Остальные периоды – большие . Каждый из них содержит 2–3 ряда элементов:
4-й период (2 ряда) – K ... Kr – 18 элементов;
6-й период (3 ряда) – Сs ... Rn – 32 элемента. В этот период входит ряд лантаноидов.
Группа – вертикальный ряд химических элементов. Всего групп восемь. Каждая группа состоит из двух подгрупп: главной подгруппы и побочной подгруппы . Например:
Главную подгруппу образуют химические элементы малых периодов (например, N, P) и больших периодов (например, As, Sb, Bi).
Побочную подгруппу образуют химические
элементы только больших периодов (например, V, Nb,
Ta).
Визуально эти подгруппы различить легко. Главная подгруппа «высокая», она начинается с 1-го или 2-го периода. Побочная подгруппа – «низкая», начинается с 4-го периода.
Итак, каждый химический элемент периодической системы имеет свой адрес: период, группу, подгруппу, порядковый номер.
Например, ванадий V – это химический элемент 4-го периода, V группы, побочной подгруппы, порядковый номер 23.
Задание 3.1. Укажите период, группу и подгруппу для химических элементов с порядковыми номерами 8, 26, 31, 35, 54.
Задание 3.2. Укажите порядковый номер и название химического элемента, если известно, что он находится:
а) в 4-м периоде, VI группе, побочной подгруппе;
б) в 5-м периоде, IV группе, главной подгруппе.
Каким образом можно связать сведения о положении элемента в периодической системе со строением его атома?
Атом состоит из ядра (оно имеет положительный заряд) и электронов (они имеют отрицательный заряд). В целом атом электронейтрален.
Положительный заряд ядра атома равен порядковому номеру химического элемента.
Ядро атома – сложная частица. В ядре сосредоточена почти вся масса атома. Поскольку химический элемент – совокупность атомов с одинаковым зарядом ядра, то около символа элемента указывают следующие его координаты:

По этим данным можно определить состав ядра. Ядро состоит из протонов и нейтронов.
Протон p имеет массу 1 (1,0073 а. е. м.) и заряд +1. Нейтрон n заряда не имеет (нейтрален), а масса его приблизительно равна массе протона (1,0087 а. е. м.).
Заряд ядра определяют протоны. Причем число протонов равно (по величине) заряду ядра атома , т.е. порядковому номеру .
Число нейтронов N определяют по разности между величинами: «масса ядра» А и «порядковый номер» Z . Так, для атома алюминия:
N = А – Z = 27 –13 = 14n ,

Задание 3.3. Определите состав ядер атомов, если химический элемент находится в:
а) 3-м периоде, VII группе, главной подгруппе;
б) 4-м периоде, IV группе, побочной подгруппе;
в) 5-м периоде, I группе, главной подгруппе.
Внимание! При определении массового числа ядра атома приходится округлять атомную массу, указанную в периодической системе. Так поступают потому, что массы протона и нейтрона практически целочисленны, а массой электронов можно пренебречь.
Определим, какие из приведенных ниже ядер принадлежат одному и тому же химическому элементу:
А (20р + 20n ),
Б (19р + 20n ),
В (20р + 19n ).
Атомам одного химического элемента принадлежат ядра А и В, поскольку они содержат одинаковое число протонов, т. е. заряды этих ядер одинаковые. Исследования показывают, что масса атома не оказывает существенного влияния на его химические свойства.
Изотопами называют атомы одного и того же химического элемента (одинаковое число протонов), различающиеся массой (разное число нейтронов).
Изотопы и их химические соединения отличаются друг от друга по физическим свойствам, но химические свойства у изотопов одного химического элемента одинаковы. Так, изотопы углерода-14 (14 С) имеют такие же химические свойства, как и углерода-12 (12 С), которые входят в ткани любого живого организма. Отличие проявляется только в радиоактивности (изотоп 14 С). Поэтому изотопы применяют для диагностики и лечения различных заболеваний, для научных исследований.
Вернемся к описанию строения атома. Как известно, ядро атома в химических процессах не изменяется. А что изменяется? Переменным оказывается общее число электронов в атоме и распределение электронов. Общее число электронов в нейтральном атоме определить несложно – оно равно порядковому номеру, т.е. заряду ядра атома:
![]()
Электроны имеют отрицательный заряд –1, а масса их ничтожна: 1/1840 от массы протона.
Отрицательно заряженные электроны отталкиваются друг от друга и находятся на разных расстояниях от ядра. При этом электроны, имеющие приблизительно равный запас энергии, находятся на приблизительно равном расстоянии от ядра и образуют энергетический уровень.
Число энергетических уровней в атоме равно номеру периода, в котором находится химический элемент. Энергетические уровни условно обозначают так (например, для Al):

Задание 3.4. Определите число энергетических уровней в атомах кислорода, магния, кальция, свинца.
На каждом энергетическом уровне может находиться ограниченное число электронов:
На первом – не более двух электронов;
На втором – не более восьми электронов;
На третьем – не более восемнадцати электронов.
Эти числа показывают, что, например, на втором энергетическом уровне может находиться 2, 5 или 7 электронов, но не может быть 9 или 12 электронов.
Важно знать, что независимо от номера энергетического уровня на внешнем уровне (последнем) не может быть больше восьми электронов. Внешний восьмиэлектронный энергетический уровень является наиболее устойчивым и называется завершенным. Такие энергетические уровни имеются у самых неактивных элементов – благородных газов.
Как определить число электронов на внешнем уровне остальных атомов? Для этого существует простое правило: число внешних электронов равно:
Для элементов главных подгрупп – номеру группы;
Для элементов побочных подгрупп оно не может быть больше двух.
Например (рис. 5):
Задание 3.5. Укажите число внешних электронов для химических элементов с порядковыми номерами 15, 25, 30, 53.
Задание 3.6. Найдите в периодической системе химические элементы, в атомах которых имеется завершенный внешний уровень.
Очень важно правильно определять число внешних электронов, т.к. именно с ними связаны важнейшие свойства атома. Так, в химических реакциях атомы стремятся приобрести устойчивый, завершенный внешний уровень (8е ). Поэтому атомы, на внешнем уровне которых мало электронов, предпочитают их отдать.
Химические элементы, атомы которых способны только отдавать электроны, называют металлами . Очевидно, что на внешнем уровне атома металла должно быть мало электронов: 1, 2, 3.
Если на внешнем энергетическом уровне атома много электронов, то такие атомы стремятся принять электроны до завершения внешнего энергетического уровня, т. е. до восьми электронов. Такие элементы называют неметаллами .
В о п р о с. К металлам или неметаллам относятся химические элементы побочных подгрупп? Почему?
О т в е т. Металлы и неметаллы главных подгрупп в таблице Менделеева отделяет линия, которую можно провести от бора к астату. Выше этой линии (и на линии) располагаются неметаллы, ниже – металлы. Все элементы побочных подгрупп оказываются ниже этой линии.
Задание 3.7. Определите, к металлам или неметаллам относятся: фосфор, ванадий, кобальт, селен, висмут. Используйте положение элемента в периодической системе химических элементов и число электронов на внешнем уровне.
Для того, чтобы составить распределение электронов по остальным уровням и подуровням, следует воспользоваться следующим а л г о р и т м о м.
1. Определить общее число электронов в атоме (по порядковому номеру).
2. Определить число энергетических уровней (по номеру периода).
3. Определить число внешних электронов (по виду подгруппы и номеру группы).
4. Указать число электронов на всех уровнях, кроме предпоследнего.
Например, согласно пунктам 1–4 для атома марганца определено:

Всего 25е ; распределили (2 + 8 + 2) = 12e ; значит, на третьем уровне находится: 25 – 12 = 13e .
Получили распределение электронов в атоме марганца:

Задание 3.8. Отработайте алгоритм, составив схемы строения атомов для элементов № 16, 26, 33, 37. Укажите, металлы это или неметаллы. Ответ поясните.
Составляя приведенные выше схемы строения атома, мы не учитывали, что электроны в атоме занимают не только уровни, но и определенные подуровни каждого уровня. Виды подуровней обозначаются латинскими буквами: s , p , d .
Число возможных подуровней равно номеру
уровня.
Первый уровень состоит из одного
s
-подуровня. Второй уровень состоит из двух
подуровней – s
и р
. Третий уровень – из
трех подуровней – s
, p
и d
.
На каждом подуровне может находиться строго ограниченное число электронов:
на s-подуровне – не больше 2е;
на р-подуровне – не больше 6е;
на d-подуровне – не больше 10е.
Подуровни одного уровня заполняются в строго определенном порядке: s p d .
Таким образом, р -подуровнь не может начать заполняться, если не заполнен s -подуровень данного энергетического уровня, и т.д. Исходя из этого правила, несложно составить электронную конфигурацию атома марганца:

В целом электронная конфигурация атома марганца записывается так:
25 Мn 1s 2 2s 2 2p 6 3s 2 3p 6 3d 5 4s 2 .
Задание 3.9. Составьте электронные конфигурации атомов для химических элементов № 16, 26, 33, 37.
Для чего необходимо составлять электронные конфигурации атомов? Для того, чтобы определять свойства этих химических элементов. Следует помнить, что в химических процессах участвуют только валентные электроны .
Валентные электроны находятся на внешнем
энергетическом уровне и незавершенном
d-подуровне предвнешнего уровня.
Определим число валентных электронов для марганца:

или сокращенно: Мn … 3d 5 4s 2 .
Что можно определить по формуле электронной конфигурации атома?
1. Какой это элемент – металл или неметалл?
Марганец – металл, т.к. на внешнем (четвертом) уровне находится два электрона.
2. Какой процесс характерен для металла?
Атомы марганца в реакциях всегда только отдают электроны.
3. Какие электроны и сколько будет отдавать атом марганца?
В реакциях атом марганца отдает два внешних электрона (они дальше всех от ядра и слабее притягиваются им), а также пять предвнешних d -электронов. Общее число валентных электронов – семь (2 + 5). В этом случае на третьем уровне атома останется восемь электронов, т.е. образуется завершенный внешний уровень.
Все эти рассуждения и заключения можно отразить при помощи схемы (рис. 6):
Полученные условные заряды атома называют степенями окисления .
Рассматривая строение атома, аналогичным способом можно показать, что типичными степенями окисления для кислорода является –2, а для водорода +1.
В о п р о с. С каким из химических элементов может образовывать соединения марганец, если учесть полученные выше степени его окисления?
О т в е т. Только с кислородом, т.к. его атом имеет противоположную по заряду степень окисления. Формулы соответствующих оксидов марганца (здесь степени окисления соответствуют валентностям этих химических элементов):
![]()
Строение атома марганца подсказывает, что большей степени окисления у марганца быть не может, т.к. в этом случае пришлось бы затрагивать устойчивый, теперь уже завершенный предвнешний уровень. Поэтому степень окисления +7 является высшей, а соответствующий оксид Мn 2 О 7 – высшим оксидом марганца.
Для закрепления всех этих понятий рассмотрим строение атома теллура и некоторые его свойства:
Как неметалл, атом Te может принять 2 электрона до завершения внешнего уровня и отдать «лишние» 6 электронов:

Задание 3.10. Изобразите электронные конфигурации атомов Nа, Rb, Cl, I, Si, Sn. Определите свойства этих химических элементов, формулы их простейших соединений (с кислородом и водородом).
Практические выводы
1. В химических реакциях участвуют только валентные электроны, которые могут находиться только на двух последних уровнях.
2. Атомы металлов могут только отдавать валентные электроны (все или несколько), принимая положительные степени окисления.
3. Атомы неметаллов могут принимать электроны (недостающие – до восьми), приобретая при этом отрицательные степени окисления, и отдавать валентные электроны (все или несколько), при этом они приобретают положительные степени окисления.
Сравним теперь свойства химических элементов
одной подгруппы, например натрия и рубидия:
Nа...3s
1 и Rb ...5s
1 .
Что общего в строении атомов этих элементов? На внешнем уровне каждого атома по одному электрону – это активные металлы. Металлическая активность связана со способностью отдавать электроны: чем легче атом отдает электроны, тем сильнее выражены его металлические свойства.
Что удерживает электроны в атоме? Притяжение их к ядру. Чем ближе электроны к ядру, тем сильнее они притягиваются ядром атома, тем труднее их «оторвать».
Исходя из этого, ответим на вопрос: какой элемент – Nа или Rb – легче отдает внешний электрон? Какой из элементов является более активным металлом? Очевидно, рубидий, т.к. его валентные электроны находятся дальше от ядра (и слабее удерживаются ядром).
Вывод. В главных подгруппах сверху вниз металлические свойства усиливаются , т.к. возрастает радиус атома, и валентные электроны слабее притягиваются к ядру.
Сравним свойства химических элементов VIIa группы: Cl …3s 2 3p 5 и I …5s 2 5p 5 .
Оба химических элемента – неметаллы, т.к. до завершения внешнего уровня не хватает одного электрона. Эти атомы будут активно притягивать недостающий электрон. При этом чем сильнее притягивает атом неметалла недостающий электрон, тем сильнее проявляются его неметаллические свойства (способность принимать электроны).
За счет чего происходит притяжение электрона? За счет положительного заряда ядра атома. Кроме того, чем ближе электрон к ядру, тем сильнее их взаимное притяжение, тем активнее неметалл.
В о п р о с. У какого элемента сильнее выражены неметаллические свойства: у хлора или йода?
О т в е т. Очевидно, у хлора, т.к. его валентные электроны расположены ближе к ядру.
Вывод. Активность неметаллов в подгруппах сверху вниз убывает , т.к. возрастает радиус атома и ядру все труднее притянуть недостающие электроны.
Сравним свойства кремния и олова: Si …3s 2 3p 2 и Sn …5s 2 5p 2 .
На внешнем уровне обоих атомов по четыре электрона. Тем не менее эти элементы в периодической системе находятся по разные стороны от линии, соединяющей бор и астат. Поэтому у кремния, символ которого находится выше линии В–At, сильнее проявляются неметаллические свойства. Напротив, у олова, символ которого находится ниже линии В–At, сильнее проявляются металлические свойства. Это объясняется тем, что в атоме олова четыре валентных электрона удалены от ядра. Поэтому присоединение недостающих четырех электронов затруднено. В то же время отдача электронов с пятого энергетического уровня происходит достаточно легко. Для кремния возможны оба процесса, причем первый (прием электронов) преобладает.
Выводы по главе 3. Чем меньше внешних электронов в атоме и чем дальше они от ядра, тем сильнее проявляются металлические свойства.
Чем больше внешних электронов в атоме и чем ближе они к ядру, тем сильнее проявляются неметаллические свойства.
Основываясь на выводах, сформулированных в этой главе, для любого химического элемента периодической системы можно составить «характеристику».
Алгоритм описания свойств
химического элемента по его положению
в периодической системе
1. Составить схему строения атома, т.е. определить состав ядра и распределение электронов по энергетическим уровням и подуровням:
Определить общее число протонов, электронов и нейтронов в атоме (по порядковому номеру и относительной атомной массе);
Определить число энергетических уровней (по номеру периода);
Определить число внешних электронов (по виду подгруппы и номеру группы);
Указать число электронов на всех энергетических уровнях, кроме предпоследнего;
2. Определить число валентных электронов.
3. Определить, какие свойства – металла или неметалла – сильнее проявляются у данного химического элемента.
4. Определить число отдаваемых (принимаемых) электронов.
5. Определить высшую и низшую степени окисления химического элемента.
6. Составить для этих степеней окисления химические формулы простейших соединений с кислородом и водородом.
7. Определить характер оксида и составить уравнение его реакции с водой.
8. Для указанных в пункте 6 веществ составить уравнения характерных реакций (см. главу 2).
Задание 3.11. По приведенной выше схеме составить описания атомов серы, селена, кальция и стронция и свойства этих химических элементов. Какие общие свойства проявляют их оксиды и гидроксиды?
Если вы выполнили упражнения 3.10 и 3.11, то легко заметить, что не только атомы элементов одной подгруппы, но и их соединения имеют общие свойства и похожий состав.
Периодический закон Д.И.Менделеева: свойства химических элементов, а также свойства простых и сложных веществ, образованных ими, находятся в периодической зависимости от заряда ядер их атомов.
Физический смысл периодического закона: свойства химических элементов периодически повторяются потому, что периодически повторяются конфигурации валентных электронов (распределение электронов внешнего и предпоследнего уровней).
Так, у химических элементов одной и той же подгруппы одинаковое распределение валентных электронов и, значит, похожие свойства.
Например, у химических элементов пятой группы пять валентных электронов. При этом в атомах химических элементов главных подгрупп – все валентные электроны находятся на внешнем уровне: … ns 2 np 3 , где n – номер периода.
У атомов элементов побочных подгрупп на внешнем уровне находятся только 1 или 2 электрона, остальные – на d -подуровне предвнешнего уровня: … (n – 1)d 3 ns 2 , где n – номер периода.
Задание 3.12. Составьте краткие электронные формулы для атомов химических элементов № 35 и 42, а затем составьте распределение электронов в этих атомах по алгоритму. Убедитесь, что ваше предсказание сбылось.
Упражнения к главе 3
1. Сформулируйте определения понятий «период», «группа», «подгруппа». Что общего у химических элементов, которые составляют: а) период; б) группу; в) подгруппу?
2. Что такое изотопы? Какие свойства – физические или химические – совпадают у изотопов? Почему?
3. Сформулируйте периодический закон Д.И.Менделеева. Поясните его физический смысл и проиллюстрируйте примерами.
4. В чем проявляются металлические свойства химических элементов? Как они изменяются в группе и в периоде? Почему?
5. В чем проявляются неметаллические свойства химических элементов? Как они изменяются в группе и в периоде? Почему?
6. Составьте краткие электронные формулы химических элементов № 43, 51, 38. Подтвердите свои предположения описанием строения атомов этих элементов по приведенному выше алгоритму. Укажите свойства этих элементов.
7. По кратким электронным формулам
а) …4s 2 4p 1 ;
б) …4d 1 5s 2 ;
в) …3d 5 4s 1
определите положение соответствующих химических элементов в периодической системе Д.И.Менделеева. Назовите эти химические элементы. Свои предположения подтвердите описанием строения атомов этих химических элементов по алгоритму. Укажите свойства этих химических элементов.
Продолжение следует
1 (2 балла). Распределение электронов по энергетическим уровням в атоме калия:А. 2е, 8е, 8е, 1е В. . 2е, 8е,
18е, 8е, 1е
Б. 2е, 1е Г. 2е, 8е, 1е
2 (2 балла). Число электронов на внешнем электронном слое у атома алюминия:
А. 1 Б. 2 В. 3 Г.4
3 (2 балла). Простое вещество с наиболее ярко выраженными металлическими свойствами:
А. Кальций Б. Барий В. Стронций Г. Радий
4 (2 балла). Вид химической связи в простом веществе - алюминий:
А. Ионная Б. Ковалентная полярная
В. Металлическая Г. Ковалентная неполярная
5 (2 балла). Число энергетических уровней у элементов одной подгруппы сверху вниз:
А. Изменяется периодически. Б. Не изменяется.
В. Увеличивается. Г. Уменьшается.
6 (2 балла). Атом лития отличается от иона лития:
А. 3арядом ядра. Б. Числом электронов на внешнем энергетическом уровне.
В. Числом протонов. Г. Числом нейтронов.
7 (2 балла.). Наименее энергично реагирует с водой:
А. Барий. В. Магний.
Б. Кальций. Г. Стронций
8 (2 балла). С раствором серной кислоты не взаимодействует:
А. Алюминий. В. Натрий
Б. Магний. Г. Медь
9 (2 балла). Гидроксид калия не взаимодействует с веществом, формула которого:
А. Na2O В. АlСl3
Б. Р2O5 Г. Zn(NO3)2
10 (2 балла). Ряд, в котором все вещества реагируют с железом:
А. НСl, СО2, СО
Б. CO2, HCl, S
В. Н2, O2, СаO
Г. O2, СuSO4, Н2SO4
11 (9 баллов). Предложите три способа получения гидроксида натрия. Ответ подтвердите уравнениями реакций.
12 (6 баллов). Осуществите цепочку химических превращений, составив уравнения реакций в молекулярном и ионном видах, назовите продукты реакций:
FeCl2 → Fe(OH)2 → FeSO4 → Fe(OH)2
13 (6 баллов). Как, используя любые реактивы (вещества) и цинк, получить его оксид, основание, соль? Составьте уравнения реакций в молекулярном виде.
14 (4 балла). Составьте уравнение химической реакции взаимодействия лития с азотом. Определите восстановитель и окислитель в этой реакции
определить по:
A. номером группы;
Б. номеру периода;
B. порядковым номером.
4. Какая из характеристик химических элементов не меняется в главных подгруппах:
А радиус атома;
Б число электронов на внешнем уровне;
В. число энергетических уровней.
5. Общее у строении атомов элементов с порядковыми номерами 7 и 15:
A. число электронов на внешнем уровне, Б. заряд ядра;
B. число энергетических уровней.
Установите соответствие между символом химичесого элемента (в заданном порядке) и числом электронов на внешнем энергетическом уровне его атома.Из буквСоответствующих правильным ответам, вы составите название установки, которая позволит человечеству еще глубже познать строение атома(9 букв).
Число е на Символ элемента
Энергетическом
уровне Mg Si I F C Ba Sn Ca Br
2 к а п о л й с е м
4 а о в к а т д ч я
7 в й л л н г о л р
1 (3 балла). Распределение электронов по энергетическим уровням в атоме натрия-А. 2 ē, 1 ē Б. 2 ē, 4 ē В. 2 ē, 8 ē, 1ē. Г. 2 ē, 8 ē, 3ē.
2 (4 балла) Номер периода в Периодической системе Д. И. Менделеева, в котором нет химических элементов-металлов: А. 1. Б. 2. В. 3. Г. 4.
3 (3 балла). Вид химической связи в простом веществе кальции:
A. Ионная. Б. Ковалентная полярная. B. Ковалентная неполярная. Г. Металлическая.
4 (3 балла). Простое вещество с наиболее ярко выраженными металлическими свойствами:
А. Алюминий. Б. Кремний. В. Магний. Г. Натрий.
5 (3 балла). Радиус атомов элементов 2-го периода с увеличением заряда ядра от щелочного металла к галогену: A.Изменяется периодически. Б. Не изменяется. B. Увеличивается. Г. Уменьшается.
6 (3 балла). Атом магния отличается от иона магния:
A. Зарядом ядра. Б. Зарядом частицы. B. Числом протонов. Г. Числом нейтронов.
7 (3 балла). Наиболее энергично реагирует с водой:
А. Калий. Б. Литий. В. Натрий. Г. Рубидий.
8 (3 балла). С разбавленной серной кислотой не взаимодействует:
А. Алюминий. Б. Барий. В. Железо. Г. Ртуть.
9 (3 балла). Гидроксид бериллия не взаимодействует с веществом, формула которого:
A. NaOH(p р). Б. NaCl(p_p). В. НС1(р_р). Г. H2SО4.
10 (3 балла). Ряд, в котором все вещества реагируют с кальцием:
А. СО2, Н2, НС1. В. NaOH, Н2О, НС1. Б. С12, Н2О, H2SО4. Г. S, H2SО4, SО3.
ЧАСТЬ Б. Задания со свободным ответом
11 (9 баллов). Предложите три способа получения сульфата железа (II). Ответ подтвердите уравнениями реакций.
12 (6 баллов). Определите вещества X, Y, Z, запишите их химические формулы.
Fe(OH)3(t)= X(+HCl)= Y(+NaOH)=Z(t) Fe2О3
13 (6 баллов). Как, используя любые реактивы (вещества) и алюминий, получить оксид, амфотерный гидроксид? Составьте уравнения реакций в молекулярном виде.
14 (4 балла). Расположите металлы: медь, золото, алюминий, свинец в порядке увеличения плотности.
15 (5 баллов). Рассчитайте массу металла, полученного из 160 г оксида меди (II).
ЭНЕРГЕТИЧЕСКИЕ УРОВНИ
| Наименование параметра | Значение |
| Тема статьи: | ЭНЕРГЕТИЧЕСКИЕ УРОВНИ |
| Рубрика (тематическая категория) | Образование |
СТРОЕНИЕ АТОМА
1. Развитие теории строения атома. С
2. Ядро и электронная оболочка атома. С
3. Строение ядра атома. С
4. Нуклиды, изотопы, массовое число. С
5. Энергетические уровни.
6. Квантово-механическое объяснение строения.
6.1. Орбитальная модель атома.
6.2. Правила заполнения орбиталей.
6.3. Орбитали с s-электронами (атомные s-орбитали).
6.4. Орбитали с p-электронами (атомные p-орбитали).
6.5. Орбитали с d- f-электронами
7. Энергетические подуровни многоэлектронного атома. Квантовые числа.
ЭНЕРГЕТИЧЕСКИЕ УРОВНИ
Строение электронной оболочки атома определяется различным запасом энергииотдельных электронов в атоме. В соответствии с моделью атома Бора электроны могут занимать в атоме положения, которым отвечают точно определенные (квантованные) энергетические состояния. Эти состояния называются энергетическими уровнями.
Число электронов, которые могут находиться на отдельном энергетическом уровне, определяется формулой 2n 2 , где n –номер уровня, который обозначается арабскими цифрами 1 – 7. Максимальное заполнение первых четырех энергетических уровней в. соответствии с формулой 2n 2 составляет: для первого уровня – 2 электрона, для второго – 8, для третьего –18 и для четвертого уровня – 32 электрона. Максимальное заполнение электронами более высоких энергетических уровней в атомах известных элементов не достигнуто.
Рис. 1показывает заполнение электронами энергетических уровней первых двадцати элементов (от водорода Н до кальция Са, черные кружки). Заполняя в указанном порядке энергетические уровни, получают простейшие модели атомов элементов, при этом соблюдают порядок заполнения (снизу вверх и слева направо по рисунку) таким образом, пока последний электрон не укажет на символ соответствующего элементаНа третьем энергетическом уровне М (максимальная емкость равна 18 е - )для элементов Nа – Аr содержится только 8 электронов, затем начинает застраиваться четвертый энергетический уровень N –на нем появляются два электрона для элементов К и Са. Следующие 10 электронов снова занимают уровень М (элементы Sc – Zn (не показаны), а потом продолжается заполнение уровня N еще шестью электронами (элементы Cа-Кr, белые кружки).
| Рис. 1 | Рис. 2 |
В случае если атом находится в основном состоянии, то его электроны занимают уровни с минимальной энергией, т. е. каждый последующий электрон занимает энергетически самое выгодное положение, такое, как на рис. 1. При внешнем воздействии на атом, связанном с передачей ему энергии, к примеру путем нагревания, электроны переводятся на более высокие энергетические уровни (рис. 2). Такое состояние атома принято называть возбужденным. Освободившееся на нижнем энергетическом уровне место заполняется (как выгодное положение) электроном с более высокого энергетического уровня. При переходе электрон отдает неĸᴏᴛᴏᴩᴏᴇ количество энергии, ĸᴏᴛᴏᴩᴏᴇ соответствует энергетической разности между уровнями. В результате электронных переходов возникает характерное излучение. по спектральным линиям поглощаемого (излучаемого) света можно сделать количественное заключение об энергетических уровнях атома.
В соответствии с квантовой моделью атома Бора электрон, имеющий определенное энергетическое состояние, движется в атоме по круговой орбите. Электроны с одинаковым запасом энергии находятся на равных расстояниях от ядра, каждому энергетическому уровню отвечает свой набор электронов, названный Бором электронным слоем. Τᴀᴋᴎᴍ ᴏϬᴩᴀᴈᴏᴍ, по Бору электроны одного слоя двигаются по шаровой поверхности, электроны следующего слоя по другой шаровой поверхности. все сферы вписаны одна в другую с центром, отвечающим атомному ядру.
ЭНЕРГЕТИЧЕСКИЕ УРОВНИ - понятие и виды. Классификация и особенности категории "ЭНЕРГЕТИЧЕСКИЕ УРОВНИ" 2017, 2018.
Сегодня поведаем о том, что такое энергетический уровень атома, когда человек сталкивается с этим понятием, и где оно применяется.
Школьная физика
Люди впервые встречаются с естественными науками в школе. И если на седьмом году обучения дети еще находят новые знания по биологии и химии интересными, то в старших классах их начинают бояться. Когда приходит черед атомной физики, уроки по этой дисциплине уже внушают только отвращение к непонятным задачам. Однако стоит помнить, что у всех открытий, которые сейчас превратились в скучные школьные предметы, нетривиальная история и целый арсенал полезных применений. Узнавать, как устроен мир - это как открывать шкатулку с чем-то интересным внутри: всегда хочется найти потайное отделение и обнаружить там еще одно сокровище. Сегодня мы расскажем об одном из базовых физики, строении вещества.
Неделимый, составной, квантовый
С древнегреческого языка слово «атом» переводится как «неделимый, наименьший». Такое представление - следствие истории науки. Некоторые древние греки и индийцы верили, что все на свете состоит из мельчайших частиц.
В современной истории были произведены намного раньше физических исследований. Ученые семнадцатого и восемнадцатого веков работали в первую очередь для увеличения военной мощи страны, короля или герцога. А чтобы создать взрывчатку и порох, надо было понять, из чего они состоят. В итоге исследователи выяснили: некоторые элементы нельзя разделить дальше определенного уровня. Значит, существуют наименьшие носители химических свойств.
Но они ошибались. Атом оказался составной частицей, а его способность изменяться носит квантовый характер. Об этом говорят и переходы энергетических уровней атома.
Положительное и отрицательное

В конце девятнадцатого века ученые вплотную подошли к изучению мельчайших частиц вещества. Например, было понятно: атом содержит как положительно, так и отрицательно заряженные составляющие. Но была неизвестна: расположение, взаимодействие, соотношение веса его элементов оставались загадкой.
Резерфорд поставил опыт по рассеянию альфа-частиц тонкой Он выяснил, что в центре атомов находятся тяжелые положительные элементы, а по краям расположены очень легкие отрицательные. Значит, носителями разных зарядов являются не похожие друг на друга частицы. Это объясняло заряд атомов: к ним можно было добавить элемент или удалить его. Равновесие, которое поддерживало нейтральность всей системы, нарушалось, и атом приобретал заряд.
Электроны, протоны, нейтроны

Позже выяснилось: легкие отрицательные частицы - это электроны, а тяжелое положительное ядро состоит из двух видов нуклонов (протонов и нейтронов). Протоны отличались от нейтронов только тем, что первые были положительно заряженными и тяжелыми, а вторые имели только массу. Изменить состав и заряд ядра сложно: для этого требуются неимоверные энергии. А вот электроном атом делится гораздо легче. Есть более электроотрицательные атомы, которые охотнее «отбирают» электрон, и менее электроотрицательные, которые скорее «отдадут» его. Так формируется заряд атома: если электронов избыток, то он отрицательный, а если недостаток - то положительный.
Длинная жизнь вселенной

Но такое строение атома озадачивало ученых. Согласно господствовавшей в те времена классической физике, электрон, который все время двигался вокруг ядра, должен был непрерывно излучать электромагнитные волны. Так как этот процесс означает потерю энергии, то все отрицательные частицы вскоре потеряли бы свою скорость и упали на ядро. Однако вселенная существует уже очень долго, а всемирной катастрофы еще не произошло. Назревал парадокс слишком старой материи.
Постулаты Бора
Объяснить несоответствие смогли постулаты Бора. Тогда это были просто утверждения, скачки в неизвестное, которые не подтверждались расчетами или теорией. Согласно постулатам, существовали в атоме энергетические уровни электронов. Каждая отрицательно заряженная частица могла находиться только на этих уровнях. Переход между орбиталями (так назвали уровни) осуществляется прыжком, при этом выделяется или поглощается квант электромагнитной энергии.
Позже открытие Планком кванта объяснило такое поведение электронов.
Свет и атом

Количество энергии, необходимой для перехода, зависит от расстояния между энергетическими уровнями атома. Чем они дальше друг от друга, тем больше выделяемый или поглощаемый квант.
Как известно, свет - это и есть квант электромагнитного поля. Таким образом, когда электрон в атоме переходит с более высокого на более низкий уровень, он творит свет. При этом действует и обратный закон: когда электромагнитная волна падает на предмет, она возбуждает его электроны, и они переходят на более высокую орбиталь.
Кроме того, энергетические уровни атома индивидуальны для каждого вида химического элемента. Узор расстояний между орбиталями различается для водорода и золота, вольфрама и меди, брома и серы. Поэтому анализ спектров испускания любого объекта (в том числе и звезды) однозначно определяет, какие вещества и в каком количестве в нем присутствуют.
Применяется этот метод невероятно широко. Спектральный анализ используется:
- в криминалистике;
- в контроле качества еды и воды;
- в производстве товаров;
- в создании новых материалов;
- в усовершенствовании технологий;
- в научных экспериментах;
- в исследовании звезд.
Этот перечень лишь примерно показывает, насколько полезным оказалось открытие электронных уровней в атоме. Электронные уровни - самые грубые, самые большие. Существуют более мелкие колебательные, и еще более тонкие вращательные уровни. Но они актуальны только для сложных соединений - молекул и твердых тел.
Надо сказать, что структура ядра до сих пор не исследована до конца. Например, нет ответа на вопрос о том, почему определенному количеству протонов соответствует именно такое число нейтронов. Ученые предполагают, что атомное ядро тоже содержит некий аналог электронных уровней. Однако до сих пор это не доказано.